
在此博客文章中,我们讨论了如何从头开始设置电化学和电池模型的一般过程。出于演示目的,我们将使用柠檬电池作为示例。
柠檬电池问题简介
柠檬电池是学校化学中的经典实验室运动。通过使用柠檬,一块铜(一分钱或一些铜线)和一块锌(例如镀锌指甲),可以建造一个可以在一件事中为小电气设备供电的电池几分钟。但是,正如许多人注意到的那样,众所周知,这些电池的适用性受到限制,在次MW范围内提供了功率。

一个带有两个电极的柠檬(左:铜;右:锌)。
建模目标
建模者应该提出的第一个问题是:建模项目的目标是什么?这似乎很容易,但是通过在这个问题上花费一些额外的思考,您通常可以节省很多时间。
对于此示例,我们将解决以下问题:是什么限制了随着时间的推移柠檬电池的功率输出,如何改进?
换句话说,我们希望将模型用作设计工具,以将瓦数提高到1 MW级别以上。其他常见的建模目标可能是减少体积,重量和/或成本。
功率输出与电极端子处的电压和电流直接相关。这意味着我们的模型需要在电池中包含电压和电压损耗的主要来源,并评估当前的费用意味着电荷的运输(离子和电子)也需要以某种方式包括在内。这个单词时间在上面的问题中也是必不可少的,因为这意味着我们需要包括瞬态。
我们可以采取什么措施来提高力量?有时最初很难知道这一点,但是考虑到设计约束的材料(柠檬,铜和锌),一个可能的假设是,我们提高性能的唯一方法是改变几何配置电极的(放置)。
总之:我们需要定义一个时间和空间依赖性模型。
化学物种和反应
现在,让我们讨论我们的模型中要包含哪些化学物种和反应。
检查柠檬的营养信息表明,电解质由柠檬酸(每升300 mm = 0.3摩尔)和抗坏血酸(3 mm)组成,均为弱酸缓冲至pH约为2个(对应于10 mm的质子浓度)。还有一个额外离子的混合,最突出的阳离子是钾(35毫米)和钙(7毫米)。在引入电极之前,柠檬中还存在一些痕量的锌(9μM)和铜(6μm)离子。除此之外,由于大部分电解质始终是电荷中性的,还有一堆阴离子(例如氯化物)可以匹配阳离子。
鉴于两个电极分别由Cu(S)和Zn(S)金属组成,并且可能溶解,因此以下电极反应似乎是合理的,可以考虑进一步分析:
在这里,在下面,陈述的平衡电位,e等式,已使用我们的营养信息的指定浓度计算NERNST等式。此时,我们还为所有反应使用双向箭头,表明反应是完全可逆的,并且可以沿任何方向进行。
由于电解质是水, 有质子和氢氧化物在整个柠檬纸浆中均匀地发生的水自生溶解引起的离子:
但是,由于酸性pH值,我们认为氢氧化浓度可以忽略不计。
在水系统中,可以形成金属氢氧化物。但是,咨询Pourbaix图对于Zn和Cu来说,对于我们的低pH值,这些不太可能在柠檬中形成。
该系统是水性的,这也意味着,取决于电极电位氧和氢可以在电极上形成或消耗:
这两个反应可能发生在两个电极上,尽管在这里我们通常假设铜电极上的动力学更快。
我们在营养清单中发现的钾和钙具有低于锌和铜的标准溶解电位,这意味着它们不会在任何范围内沉积在任何电极上。同样,氯气的演化具有高于氧气的标准潜力,因此现在也可以忽略。
多种不同的金属离子与混合电极电势的存在导致了可能的金属沉积侧反应的相当复杂的系统,尤其是在Zn电极上。例如,柠檬中的痕量铜离子或柠檬中的任何其他贵族离子都可以沉积在锌电极上。例如,这可能会改变该电极的电催化特性,这些电极沉积Cu可能会显着增加氢进化的活性。我们选择此时也忽略了这些效果,并假设金属铜和锌沉积溶解仅在其各自的电极上发生。
关于弱酸(柠檬酸和抗坏血酸),这些分子相对较大且复杂,通常会导致缓慢的动力学。我们只是假设它们不要在电极上反应。我们还忽略了与金属阳离子的弱酸的复合物的形成。至于营养清单上的其他物种(糖,脂肪等),我们现在也忽略了它们。
电解质传输
现在,我们将注意力转向电解质中的运输过程。
首先,我们需要决定电解质电荷传输和电解质电位的模型,因为电解质电势与金属中电势之间的电位差是电极反应的主要驱动力。
我们上面的结论是,存在大量离子(k+,Cl-等等)不参与电极反应。这允许支持电解质假设,这意味着不能假定电解质的电导率由于电极反应而显着变化。因此,我们可以假设恒定电导率(0.35 s/m),并使用欧姆定律的部分微分方程版本求解电解质电势。
上面的电极反应包括Cu2+,Zn2+, H+, H2,o2,因此需要在模型中以某种方式定义这些物种的浓度(化学活性)。
Zn(S)和Cu(S)分配了恒定的化学活性1,不需要进一步治疗。我们还假设电极的形状不会因金属溶解而改变。
由于与纯水(55.5 m)相比,离子浓度较低,我们可以假设电解质为稀。这意味着我们假设电解质中的物种仅与水分子相互作用,充当溶剂。
使用稀释假设,锌的传输2+和Cu2+可以使用内斯特 - 普朗克方程,我们只需要提供一个每个离子的一个扩散率/迁移率参数。
由于存在弱酸(柠檬酸和抗坏血酸),pH缓冲能力不参与电极反应,我们假设常数pH(氢浓度)。
柠檬外表面周围空气中的气体(氮,氧,二氧化碳等)可能会溶解并扩散到电解质中。在这里,我们将除氧气以外的所有气体视为惰性。假定氧与外柠檬表面的周围空气处于平衡状态。从表面上,它可能会向电极扩散,在该电极中减少。氧扩散过程也可以用Nernst – Planck方程来描述(这等于Fick的扩散定律对未充电物种的扩散定律)。由于还原反应在化学系统中的反应具有最高的平衡潜力,因此我们不必考虑氧气演化。
氢的运输在模型上有些问题。氢进化/氧化反应具有位于我们反应系统中间的平衡电位,这意味着该反应可以沿任何方向进行(取决于局部电极电位)。如果在电极上形成氢气气泡,则会构成建模并发症,因为这还引入了我们系统中的第二相(除液相外)。两相系统通常是复杂的模型,对于柠檬浆,没有直接的方法来描述气泡传输。因此,我们选择通过假设所有氢作为具有活性1的气体形成,并在有机会被氧化之前立即排出。方程式,这是通过仅允许氢反应作为还原反应(氢进化)不可逆地进行的。对于阳性(氧化/阳极)电极过电势,将反应速率设置为0。这样,该模型不必为氢浓度解决。
系统边界和几何形状的选择
当涉及锌和铜的碎片时,这些金属与柠檬浆的电导率很高,因此足以建模金属的电(电子)电位为边界条件。结果,以及上述讨论,提议的电池模型完全受电解质(柠檬的果肉)和电极表面上的反应的影响。因此,我们选择柠檬的外表面,不包括金属域,作为系统边界。
同样,在构建模型几何形状时,我们通过将柠檬切成两半来考虑对称性,以节省计算资源。
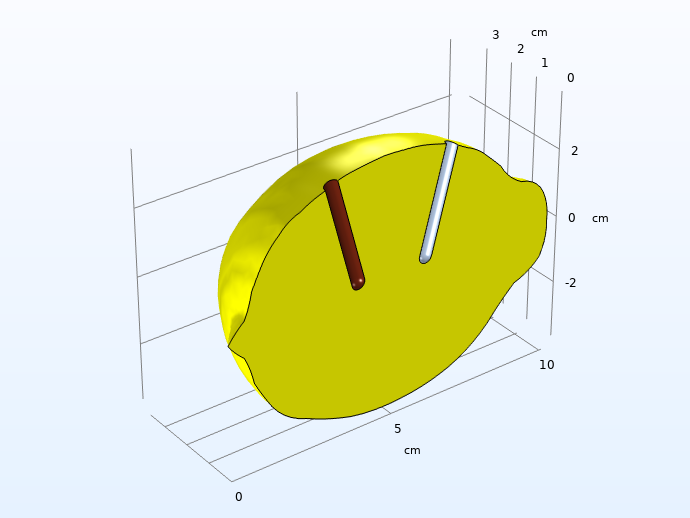
考虑对称性和电极中的高电导率后,计算域。
注意:始终建议使用最低的维度,因为这通常会节省模型开发和计算时间。对于实际的柠檬,您可以考虑在中央轴周围具有轴向对称性的2D几何形状,但是由于我们希望完全自由放置电极,因此我们必须在3D中构造模型。但是,即使对于我们的情况,仍然建议以较低维度启动建模项目,以测试不同的域方程和边界条件并确保它们收敛。例如,该模型将适合在1D上建模,并在两者之间模拟两个平面电极,但我们在此博客文章中省略了这一步骤。
在ComsolMultiphysics®中模拟柠檬电池
在下面显示的结果中,我们使用三级电流分布,支持电解质Comsol多物理学中的接口以建模柠檬电池。我们通过恒定电导率,通过NERNST-PLANCK方程的物种运输,基于内置质量行动法的电极反应来定义电荷运输,并基于内置的质量行动法管法 - 沃尔默动力学以及基于Nernst方程的平衡电位计算。
这里有一个警告:大多数参数值,尤其是对于电极动力学,用于唯一的演示目的,而不是基于文献。
在模拟中,使用的负载周期包括从初始条件(营养列表值)的1分钟休息,然后在0.5 mA处载荷1分钟,休息1分钟。
在操作过程中解释电压曲线
下图显示了所得的电压和来自仿真的电流。
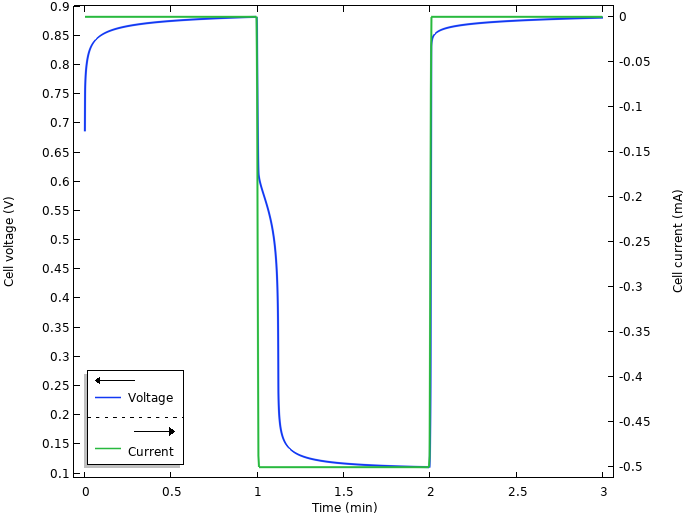
电压和电流。
最初,当电极插入柠檬中时,似乎会出现某种放松,并且在t = 1分钟时打开电流时,慢慢增加了电池电压,从而迅速从向约0.1 V的操作电压的开路电压。我们还注意到在2分钟后关闭电流后某种放松。
通过将电池电压乘以电流,我们还可以绘制电池的功率输出。
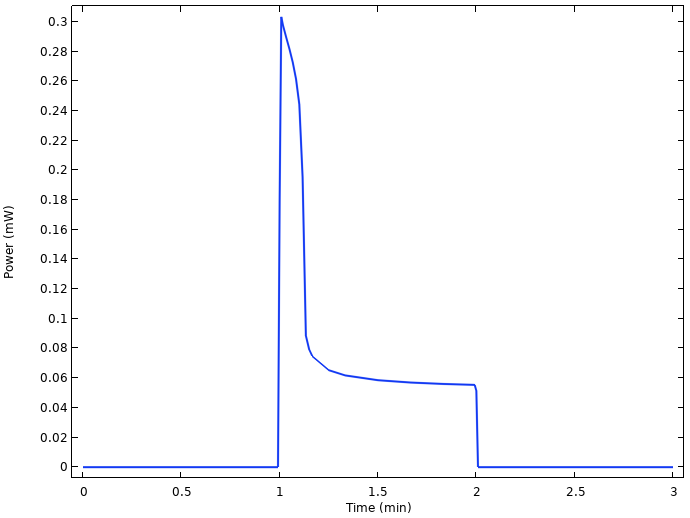
电池的功率输出。
打开负载后仅几秒钟,功率损耗从0.3到0.06 mW,与大量电压下降有关。
当电流打开时,这种巨大(对于电化学家)的巨大(对于电化学家)的背后约为0.75 V?我们通过在两个电极与时间的尖端绘制工作电极电位(与SHE)来开始分析:
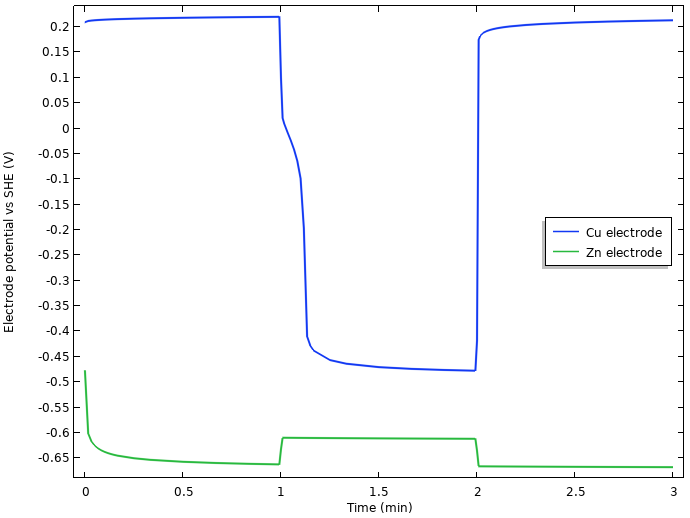
电极电势与她在指甲的尖端。
我们注意到,静止时的细胞电压的初始增加似乎与负锌电极处发生的事物有关,但是当电流负载打开时,细胞电压下降的大部分V降低似乎源于正铜电极。
绘制铜指甲表面的平均氧气浓度与下图中的时间暗示了解释。
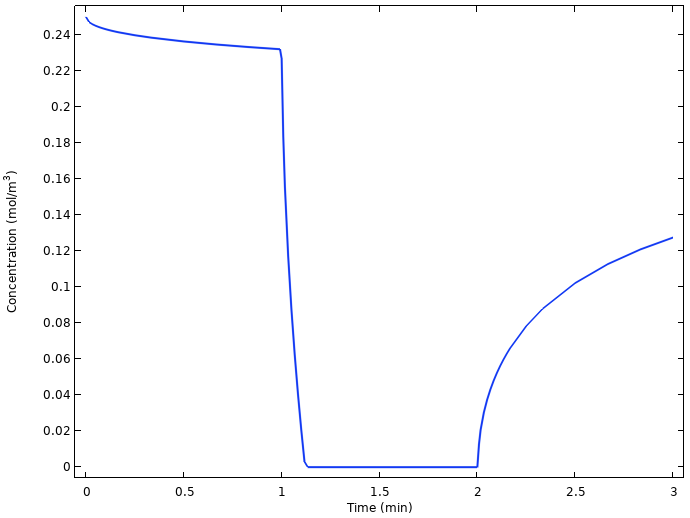
铜电极处的平均氧气浓度。
当电流打开时,铜电极处的氧气浓度会迅速降至零,并在再次关闭电流后开始放松到更高的值。原因是,一旦打开负载,氧气从柠檬表面到铜电极的缓慢扩散不足以维持电池电流。提出这一点的另一种方法是,我们正在操作电池以上的限制电流以减少氧气。
绘制整个铜指甲表面的不同电极反应的局部电流密度提供了进一步的见解。
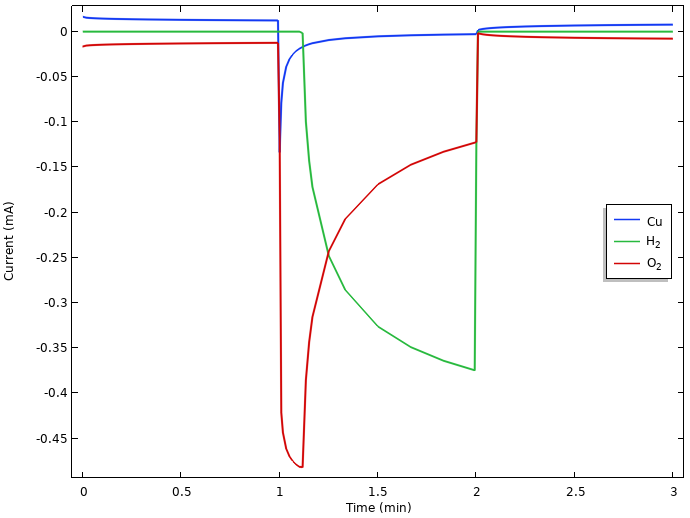
在正电极处积分的局部电流密度。
如果我们在上图的最初休息时间内密切检查电流,我们可以看到铜以与氧气减小的(一个小负电流)相同的速率溶解(小正电流)。这表明在静止期间存在连续的铜腐蚀。初始休息期间不存在氢的演化。这是由于氢进化的平衡潜力低于所得的混合电极电位,这在铜溶解和还原氧的平衡电位之间达到了一个值。(但是,如果在电极处存在氢气,则将被氧化,但是如上所述,氢气在任何时候都不存在于柠檬中。)
当电流打开时,我们看到氧还原电流的初始浪涌,然后随着氧气耗尽而倒退。由于由于我们操作电池的方式,所有电流都被限制在总和至0.5 mA电池负载,因此当电极从氧气中耗尽时,电势会下降,直到其达到低于氢的电极电位,然后可以介入提供所需的减少电流。由于水的自动解反应和高水分,电极处有大量的质子供应,其限制电流用于氢进化阶的数量级,高于氧气还原。我们还注意到,当电极的电势在负载期间掉落时,铜开始沉积。
因此,我们从静止时铜溶解 - 氧降低的电极电势过渡到氢进化为延长载荷的氢。从剩下的电位约0.2 V,而在负载期间,大约0.45 v的操作电位的大量下降可以通过氢进化的平衡潜力明显低于减少氧气的降低。动力学也在由此产生的值中发挥了一定作用,但是我们目前将其排除在外。
负电极和电池容量的自我放电
下图显示了负电极处各个电极反应的局部电流密度。
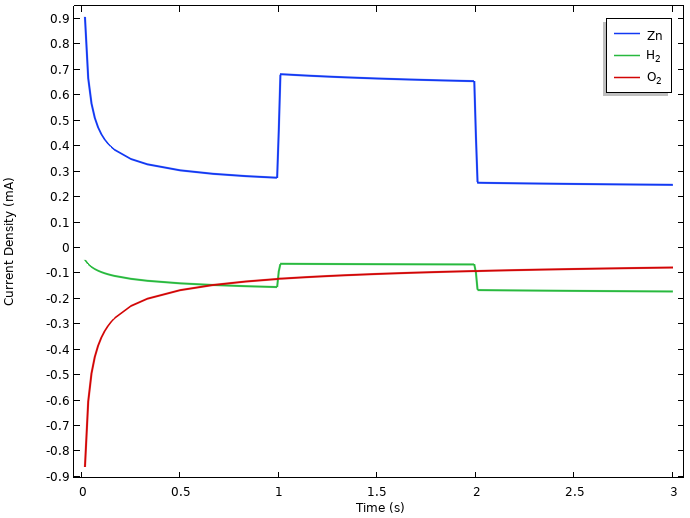
负电极处的局部电流密度。
在这里,还原和氢的进化都会导致静止锌溶解。(最初的放松现象与所有这些反应之间的相互作用有关,但我们不会在这里进一步讨论。)
在负载期间,锌溶解增加以匹配0.5 Ma细胞电流,再加上氧还原和氢进化电流。
连续的锌溶解表明,我们放入柠檬中的锌金属的初始质量将确定电池的能力,因为在正电极下,水自动溶解反应将为我们提供几乎无限的质子来源氢进化反应。但是,我们可以从电池中排出的确切的放大器小时数将取决于负载和自降压反应之间的相互作用。
评估电压损耗
在负载期间,我们在模型中有三个主要的电压损耗来源:
- 电解质中的欧姆滴
- 激活驱动锌溶解在负电极上的激活过电势
- 驱动正极电极上氢进化反应(或还原氧)的激活过电势
首先,我们将电解质的欧姆滴绘制到负载脉冲30秒钟。
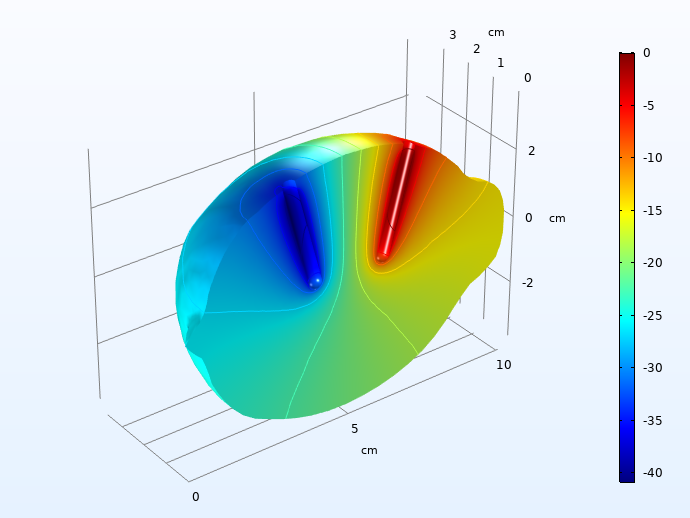
电解质欧姆滴(MV),进入电荷脉冲30秒。
40 mV的电压下降很大,但不大。
接下来,我们绘制Zn溶解在负电极上的局部超电势,以及在正电极上的氢进化。
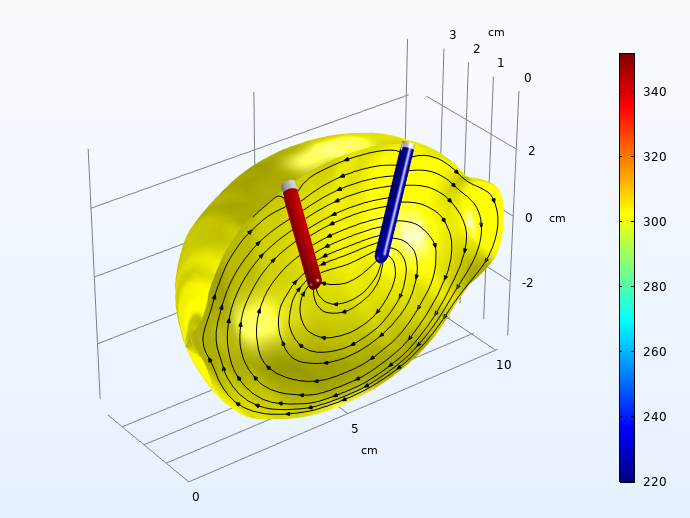
氢(左)和锌溶解(右)激活过电势(MV,绝对值),进入电荷脉冲30秒。流线描绘了沿对称平面的电解质电流。
两个电极上的激活过电势总和到达载荷脉冲30秒钟约0.5 v。这些高于电解质中电荷传输的欧姆损失。
增强功率输出
现在,我们返回我们的原始建模项目目标,以查看是否可以提高电池的功率输出。
改善Zn电极上的内在电极动力学,对于我们的一组参数值对细胞极化产生了最大的影响,在不改变非常电极或电解质的情况下很难实现。但是,通过增加可用电极 - 电解质界面面积的量也可以改善催化活性。这样做的原因是,所有电流都必须在每个电极上传递电极 - 电解质界面,并且与电极反应相关的电压损耗的局部电流密度越高。通过增加电极反应的可用面积,每个电极区域的局部电流密度就会降低,进而又会损耗相关的电压损耗。
由于我们在柠檬中有大量的空间,因此电极的几何区域(或更多的指甲)应该是提高性能的可行方法。但是,这也会增加自我解脱,因为这也与活动电极区域直接相关。
如果可以降低电解质的欧姆下降,细胞性能也将略微受益。实现这一目标的一种方法是简单地将电极彼此靠近。但是,我们必须谨慎行事,因为我们可以增加不需要的Cu沉积对Zn电极的影响,这可能会使Zn电极动力学恶化。但是,我们尚未在模型中包含此类效果。
圣杯将是0.5 V电压的提升(请参阅上图)可以以某种方式利用铜电极上的氧气还原而不是氢进化。实现此目的的一种方法可能是将铜电极放置在柠檬表面上,以缩短氧气的扩散距离。
根据我们的建模结果,我们现在为柠檬电池提出以下功率优化设计。

功率优化的柠檬电池设计。
在此设计中,我们将铜指甲换成便士。我们还引入了多个电极(每对柠檬的楔子一对夫妇,总共12对夫妇)。也许应该注意的是,新设计的接线工作将需要一些敏捷的手指。
引入多种金属电极会增加整体电极表面积。这应该使我们能够以较高的总电流运行电池(原则上,我们现在正在平行运行12个电池)。引入铜色便士而不是指甲会进一步增加电极区域,但更重要的是,这还应增加位于柠檬表面的铜电极表面的量,这应该使更高的限制电流以减少氧气。
当我们为新设计进行新的模拟时,总电流为6 mA(每楔形0.5 mA),我们将获得以下细胞电压结果:
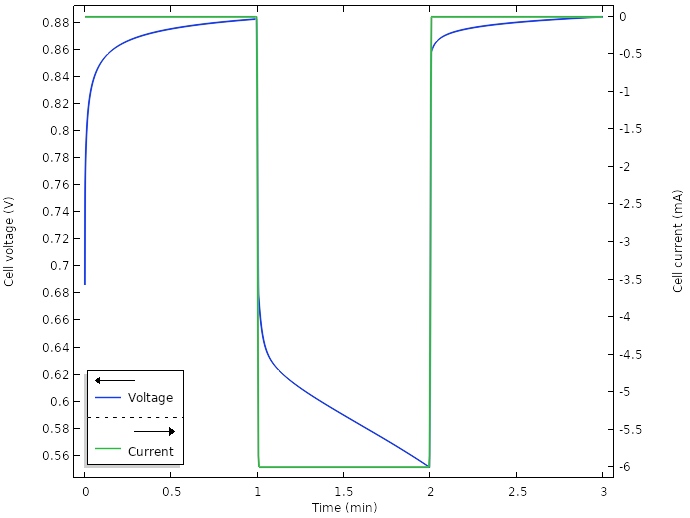
新设计的电压和电流。
相应的细胞功率揭示了我们现在能够操作远高于1 MW级别的单元格:
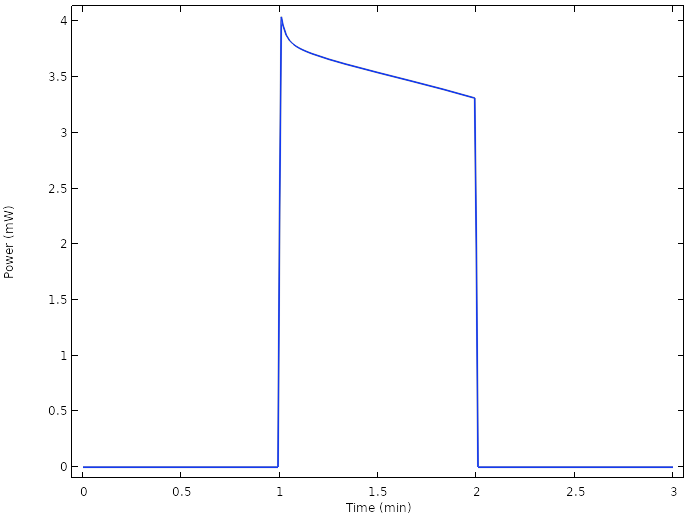
新设计的电源。
主要的贡献者是使用多个电极,但是绘制电极电位的揭示,我们已经设法增加了负载期间的潜在正电极电位超过0.5V。
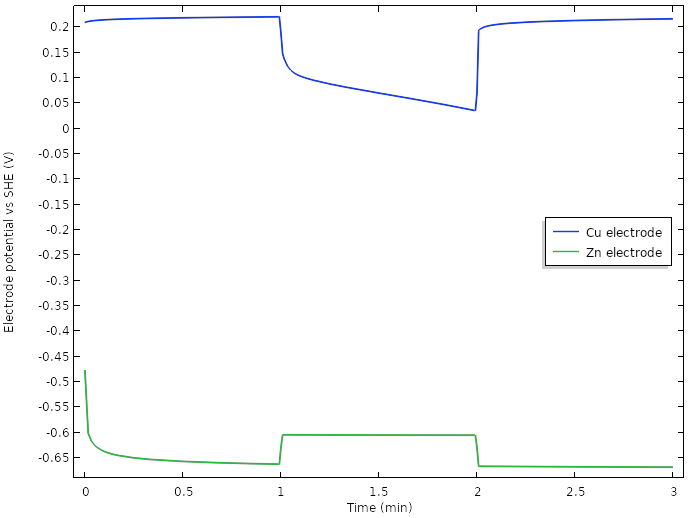
电极电位与她在电极尖端的新设计。
在铜电极上再次检查氧气浓度,发现我们现在没有随时到达电极处的氧气完全消耗。
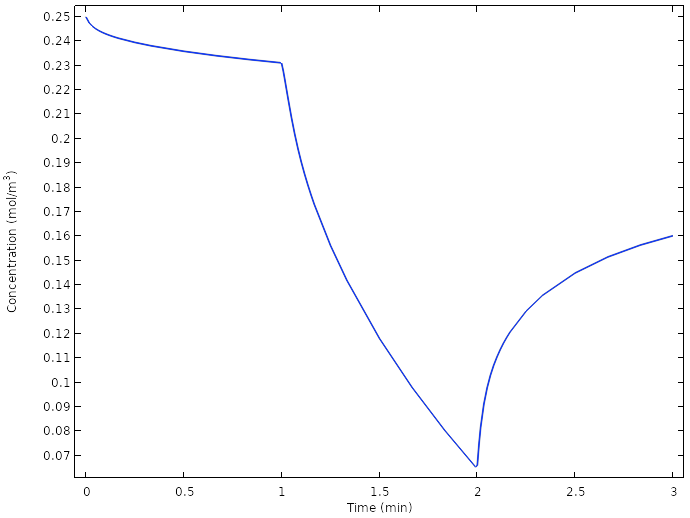
新设计的铜电极处的平均氧气浓度。
相应地,阳性电极反应电流的图表明,现在负载过程中的主电极反应是氧还原反应。
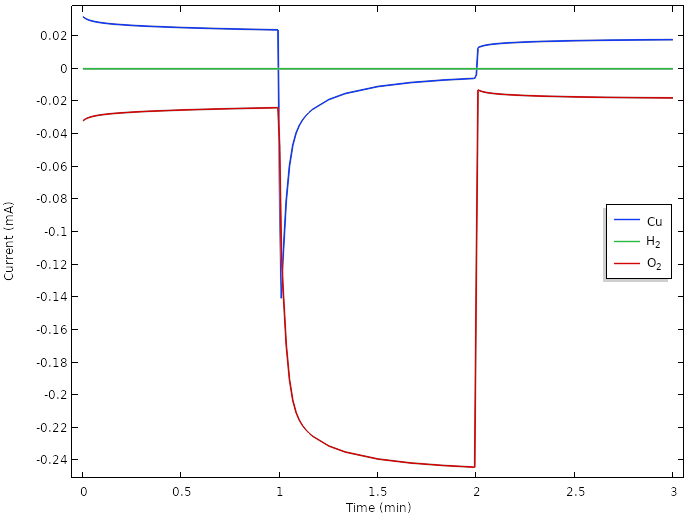
但是,氧浓度和电流随时间不断下降。实现进一步改进的一种方法可能是引入疏水多孔气体扩散介质,以促进柠檬和铜电极表面之间的氧气运输。由于气相扩散通常比液体快的速度快四到五个数量级,因此这将显着增加氧气的运输。应该如何完成此操作的详细信息将非常适合使用模型探索。可能,我们还必须将铜金属交换为更活跃的减少氧气,例如铂。但是,铂金便士往往很难获得。
然而,尽管碱性电解质是一种柠檬电池,但已经发明了这种方式。它称为锌空气电池。
下一步
对电化学建模的其他例子感兴趣?通过单击下面的按钮在应用程序库中探索更多的电化学模型。





评论(8)
Srihari Gangaraj
2020年5月20日在WFH时代,非常有趣的帖子和娱乐性。感谢分享。
Priyanshu Vishnoi
2021年2月24日在此模型中,您忽略了氢气气泡的形成。如果有一个电化学模型,即来自氢进化反应的氢浓度如此之高,以至于肯定会发生气泡?有什么方法可以使用第三纪电流分布Nernst-Plank Physics将氢气气泡形成(和运输)纳入电化学模型?
HenrikEkström
2021年2月24日是的,电流极低,因此在该模型中确实忽略了氢气气泡的形成。
有关气泡形成和由于气体演化而导致的示例,与第三纪电流分布相结合,Nernst-Planck界面,请查看//www.dvdachetez.com/model/two-phase-flow-modeling-of-copper-electrowinning-using bubbly-flow-75111
亨特·斯特拉斯曼(Hunter Strathman)
2021年10月14日可以从本教程中分享您的模型吗?我正在努力模拟电极上的多个氧化还原反应,这将非常有帮助。
HenrikEkström
2021年10月15日嗨,亨特。
该模型现在可以从中下载//www.dvdachetez.com/model/lemon-battery-86411
亨特·斯特拉斯曼(Hunter Strathman)
2021年10月15日谢谢!我认为与.mph的链接是不正确的。当我单击它时,我将其重定向到comsol.com,无需选择保存.mph文件。
HenrikEkström
2021年10月18日单击“下载应用程序”选项卡不工作?我只是在Comsol外部的计算机上测试了它,它在那里工作。
亨特·斯特拉斯曼(Hunter Strathman)
2021年10月18日是的,今天正在工作。不确定以前是什么问题。谢谢!